В предыдущем исследовании Университета Кумамото в Японии исследователи разработали метиловый эфир, конъюгированный с фолиевой кислотой-?-циклодекстрин (FA-M-?-CyD), который нацелен на рецептор фолиевой кислоты-? (FR-?) -экспрессирующие (+) опухолевые клетки посредством неизвестного аутофагического механизма. Исследователи предположили, что FA-M-?-CyD ингибировал митохондриальную активность, и начал эксперименты с этим соединением на линии клеток рака шейки матки, полученных из HeLa (клетки KB).
Исследователи впервые оценили FA-M-?-CyD путем сравнения его эффектов с действием трех других соединений, а также с контролем на сфероиды FR-? (+) КБ клетки in vitro. Они обнаружили, что FA-M-?-CyD снижает жизнеспособность раковых клеток значительно больше, чем другие соединения, благодаря его FR-?-опосредованная цитотоксичность.
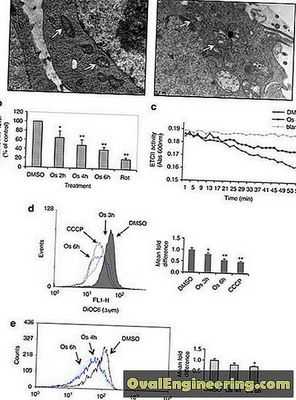
Затем исследователи определили, что FA-M-?-CyD был локализован в FR-?? (+) Митохондрии клеток KB и что он значительно увеличивает трансмембранный потенциал митохондрий по сравнению с другими протестированными соединениями. Трансмембранный потенциал митохондрий контролирует выработку энергии (АТФ) клеткой, и, кроме того, было обнаружено, что производство АТФ было значительно снижено в FR-? (+) КБ ячеек. Однако когда FR-? (-) Раковые клетки A549 обрабатывали FA-M-?-CyD, производство АТФ не изменилось.
Затем исследователи из Университета Кумамото сосредоточили внимание на эффекте, который FA-M-?-CyD влияет на продукцию АФК в клетках КБ, поскольку активные формы кислорода (АФК) часто генерируются митохондриями.
Они обнаружили, что производство ROS значительно увеличилось в FR-? (+) КБ клетки, но не были затронуты в FR-? (-) КБ ячеек. Кроме того, благодаря производству ROS в FR-? (+) КБ клетки, ФА-М-?-CyD также, по-видимому, вызывает создание аутофагической вакуоли.
Эксперименты in vivo с FA-M-?-Противоопухолевые эффекты CyD в клетках KB (FR-? (+)) использование моделей ксенотрансплантатов человека показало многообещающие. Мало того, что однократная доза соединения значительно подавляла рост опухоли, но также не было никаких серьезных побочных эффектов, что было продемонстрировано массой тела и анализами крови.
Однако для подтверждения безопасности соединения требуются дальнейшие испытания в более высоких дозах, но исследователи настроены осторожно и оптимистично.
"Одной из проблем, которые необходимо преодолеть противоопухолевым препаратам, является нарушение распределения кровеносных сосудов и перфузии крови в опухолях. Это препятствует способности препарата проникать в клетки и выполнять свою работу », — сказал профессор Арима, один из руководителей проекта. «Однако недавние исследования показали, что наночастицы размером около 12 нанометров могут легко проникать в опухолевые клетки. FA-M-?-CyD измеряли при длине волны около 10 нм, что способствует его противоопухолевым свойствам."Состав должен быть нацелен на FR-?? +. Однако есть надежда, что из него получится мощное противораковое лекарство.
Это исследование можно найти в Интернете в Международном журнале наномедицины Dove Medical.

